PNO - Cục Quản lý Dược (Bộ Y tế) cho biết, cơ quan chức năng vừa phát hiện thêm 1 lô dầu gội do công ty chồng Đoàn Di Băng phân phối vi phạm.
| Chia sẻ bài viết: |

Ngày 11/5, bé trai 2 tuổi bị bạo hành đã được cấp giấy khai sinh tại Bệnh viện Nhi đồng 1 TPHCM.
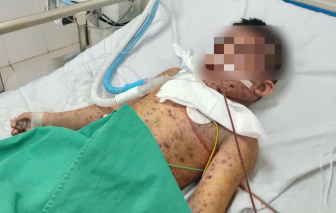
Một bé trai 6 tuổi ở Lai Châu nguy kịch vì thủy đậu biến chứng. Bác sĩ cảnh báo không chủ quan với các nốt phỏng nước thông thường.

Tiệm bánh mì liên quan đến vụ 62 người nhập viện cấp cứu bị xử phạt 18 triệu đồng vì vi phạm quy định vệ sinh an toàn thực phẩm.
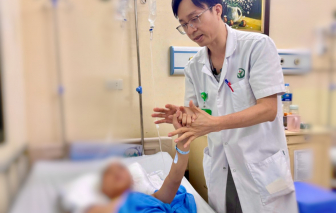
Thời điểm nhập viện, trẻ bị dao bầu đâm thẳng vào đỉnh đầu bên trái nhưng vẫn tỉnh, liệt tay phải.

Một nghiên cứu mới từ Mỹ cho thấy thói quen ăn trứng đều đặn có thể giúp bảo vệ não bộ và giảm tới 27% nguy cơ mắc bệnh Alzheimer.

Ngại đi khám bệnh nam khoa khiến nhiều người âm thầm chịu đựng bệnh trong thời gian dài, ảnh hưởng đến sức khỏe sinh lý, tâm lý và khả năng sinh sản.

Nghiên cứu cảnh báo thói quen đi ngủ không đúng giờ ở tuổi 40 có thể khiến rủi ro mắc bệnh tim mạch nghiêm trọng tăng gấp 2 lần.

Chuyên gia, nhà khoa học trong và ngoài nước thảo luận xu hướng mới về ứng dụng AI trong y học, thuốc sinh học, điều trị…

Nghiên cứu từ Úc khẳng định du lịch tích cực chính là liệu pháp tự nhiên giúp mọi người làm chậm lão hóa và duy trì năng lượng tươi trẻ.

Việc tổ chức khám sức khỏe định kỳ cho người dân cần được nghiên cứu kỹ, bảo đảm phù hợp với yêu cầu thực tiễn.

Cụ bà thường bị ói sau ăn, bụng chướng nhẹ. Khi đến bệnh viện khám, bà được bác sĩ chỉ định phẫu thuật cấp cứu.
Liệu pháp miễn dịch ngắn hạn trước phẫu thuật giúp bệnh nhân ung thư đại trực tràng sạch bóng tế bào ác tính suốt gần 3 năm sau đó.
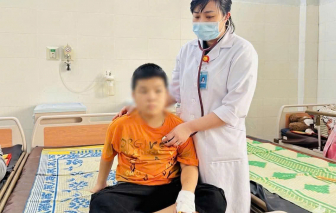
Bệnh nhi ở Quảng Ngãi được phát hiện có dị vật rỉ sét trong phổi sau nhiều năm khò khè không rõ nguyên nhân.

Tròn 2 năm kể từ ca ghép thận thành công đầu tiên, Bệnh viện đa khoa Trung ương Cần Thơ đến nay đã thực hiện thành công 20 ca ghép thận.
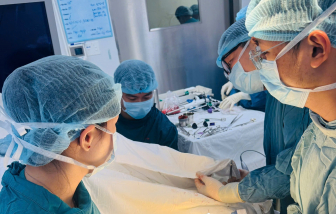
Ngay khi vừa có kết quả chấn đoán hình ảnh, các bác sĩ tại Bệnh viện Nguyễn Tri Phương lập tức đưa bệnh nhân vào phòng mổ để lấy “trứng rồng”

Trong gần hai thập niên phát triển, Mamamy theo đuổi hướng đi đặt tiêu chuẩn an toàn cao hơn mức phổ biến.

Bệnh viện Nhân dân Gia Định cơ sở 2 ra mắt phòng khám Nam khoa nhằm đáp ứng nhu cầu chăm sóc sức khỏe cho các quý ông mắc bệnh khó nói.

Thứ trưởng Bộ Y tế khẳng định phải có giải pháp dự phòng để ngăn bạo hành trẻ em từ sớm, thay vì chỉ hỗ trợ khi sự việc đã xảy ra.