PNO - Ranitidine (thường được biết đến với tên thương mại Zantac) được sử dụng trong điều trị bệnh loét dạ dày tá tràng, bệnh trào ngược dạ dày thực quản.
| Chia sẻ bài viết: |

Sau khi ăn nấm rừng, 6 người dân tại Sơn La có biểu hiện ngộ độc. Trong đó 1 ca tử vong, các trường hợp còn lại đang điều trị tích cực.

Sau vụ bé 4 tuổi tử vong ở Hà Nội và bé 2 tuổi nguy kịch tại TPHCM do bị bạo hành, Bộ Y tế yêu cầu tăng cường bảo vệ trẻ.

Do tâm lý e ngại và lo sợ, bệnh nhi đã cố chịu đựng cơn đau suốt đêm mà không thông báo cho gia đình.

Sau khi đột ngột ngã quỵ vì yếu liệt tay chân, người đàn ông được đưa đến Bệnh viện Quân Y 175 cấp cứu.

Ngày 6/4, Thủ tướng Chính phủ đã có Chỉ thị về việc tổ chức khám sức khỏe định kỳ hoặc khám sàng lọc miễn phí cho người dân.
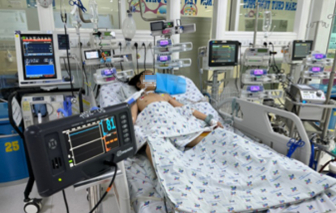
Bệnh viện Nhi Đồng Thành phố vừa cứu sống một bé gái viêm cơ tim tối cấp kèm sốc nhiễm trùng, nhiễm trùng huyết và suy đa cơ quan do phế cầu.

Trung tâm Y tế Quân dân y Đặc khu Côn Đảo đã thực hiện chạy thận nhân tạo, giúp bệnh nhân suy thận mạn được điều trị ngay tại địa phương.
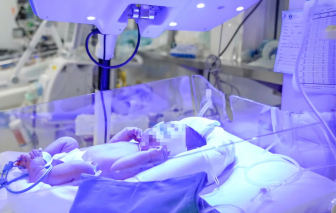
Bé trai 4 ngày tuổi phát hiện mang nhóm máu cực hiếm sau khi vàng da, thiếu máu nặng. Ca bệnh lần đầu ghi nhận tại Bệnh viện Nhi Trung ương.

Mỗi mùa thi đến không chỉ là áp lực của học sinh mà còn là “bài kiểm tra tâm lý” cho cả gia đình...
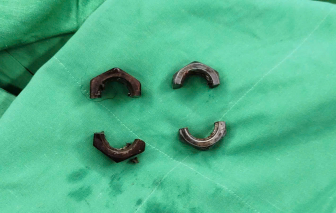
Bệnh viện đa khoa Trung ương Cần Thơ vừa phẫu thuật thành công cho bệnh nhân bị dị vật kim loại dạng đai ốc siết chặt dương vật trong thời gian dài.

Sau khi hái lá cà độc dược nấu cùng cá khô để ăn, 1 người dân bị nôn ói, nói sảng, ảo giác và kích thích mạnh, phải nhập viện cấp cứu.

Chỉ trong hơn 1 tháng, Bệnh viện Đa khoa khu vực Hướng Hóa (Quảng Trị) đã tiếp nhận 9 trường hợp ngộ độc sau khi ăn ve sầu.
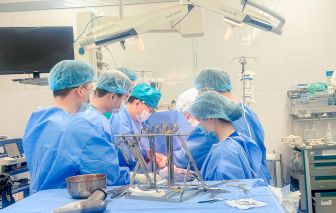
Bệnh viện Thống Nhất đã kích hoạt quy trình báo động đỏ, phẫu thuật khẩn cứu sống nam bệnh nhân bị vết thương xuyên tim nguy kịch, mất lượng máu lớn.

Mỗi người dân sẽ có một hồ sơ sức khỏe điện tử duy nhất, gắn với mã định danh cá nhân, chủ động chăm sóc sức khỏe toàn diện liên tục.
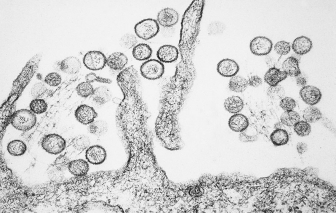
Theo thông tin của WHO, trên tàu du lịch có lịch trình từ Argentina qua Nam Đại Tây Dương, 7 người nghi nhiễm vi rút Hanta, trong đó 3 ca tử vong.

Tối 4/5, Cục An toàn thực phẩm (Bộ Y tế) đã cảnh báo về ản phẩm sữa công thức a2 Platinum Premium dành cho trẻ 0 - 12 tháng tuổi.
Nghiên cứu mới gây bất ngờ: dù lượng nước nạp vào cơ thể có tăng lên, nhưng tỉ lệ sỏi thận tái phát không hề giảm đi đáng kể...
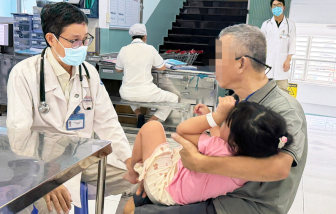
Báo Phụ nữ TPHCM trao đổi với bác sĩ Dư Tuấn Quy - Trưởng khoa Nhiễm - Thần kinh, Bệnh viện Nhi Đồng 1 về cách phòng bệnh não mô cầu.